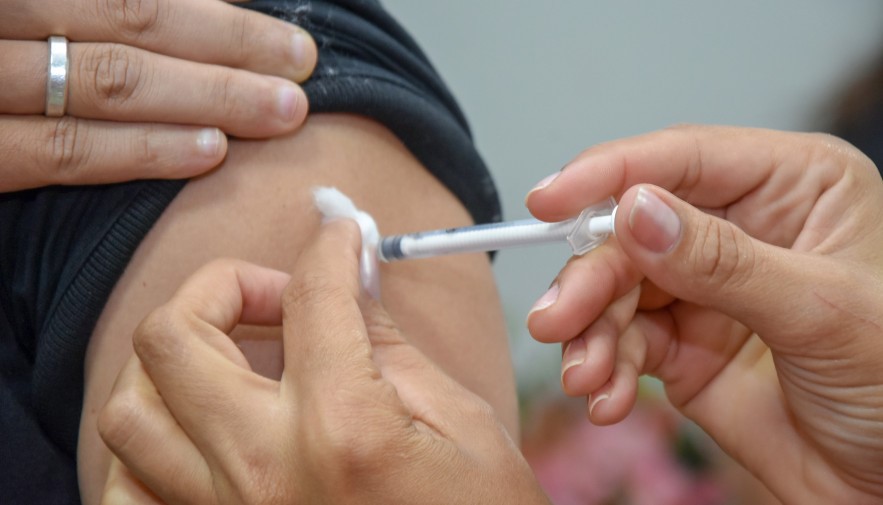
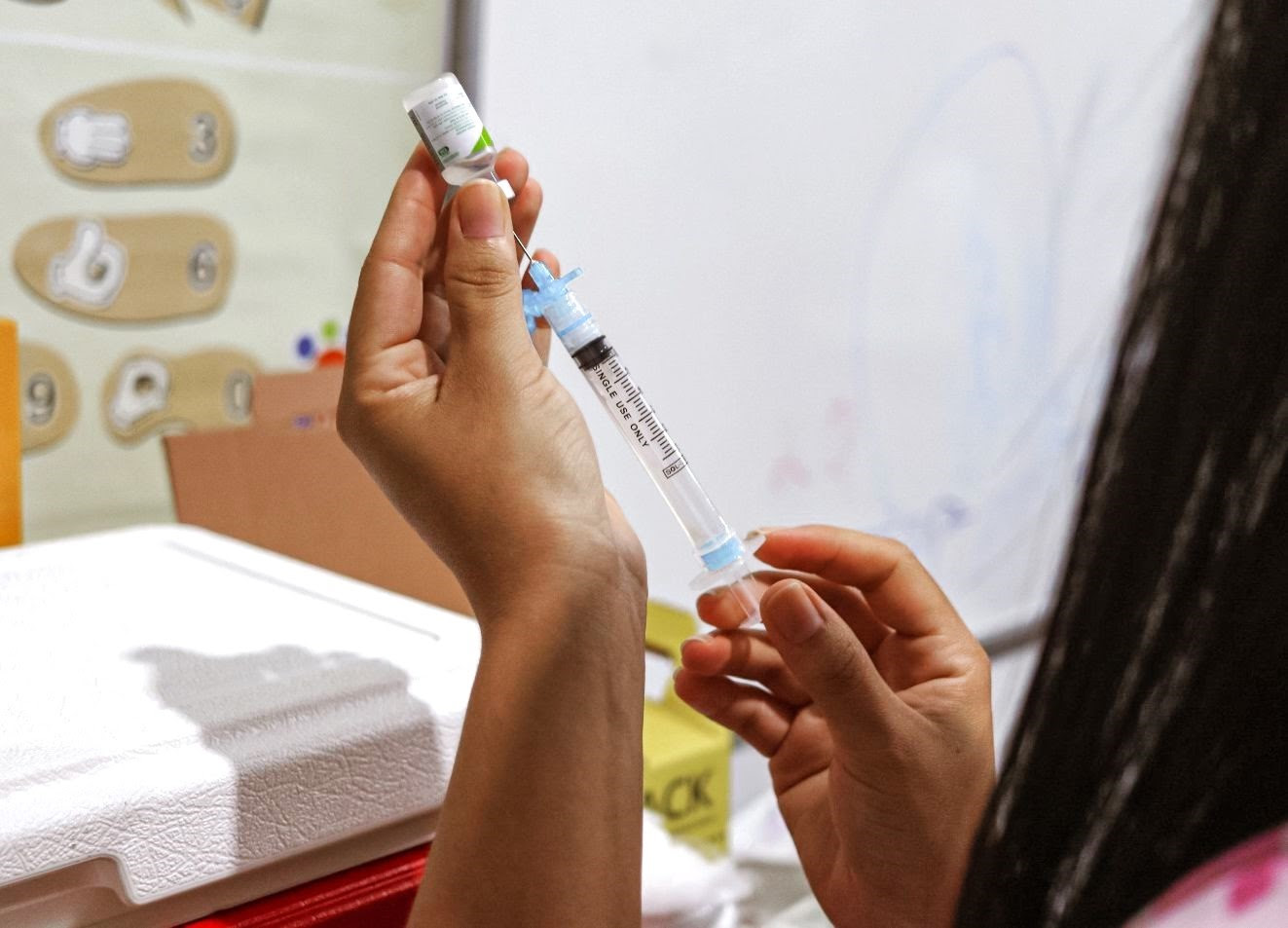
O governador do Estado do Tocantins, Mauro Carlesse, reuniu-se na manhã deste sábado, 5, com os demais governadores que compõem o Consórcio Interestadual de Desenvolvimento Sustentável da Amazônia Legal para debater a decisão tomada pela Agência Nacional de Vigilância Sanitária (Anvisa), na noite dessa sexta-feira, 4, quanto ao uso da vacina russa Sputnik V para testes no Brasil. Na reunião, realizada por videoconferência, os governadores decidiram que só vão efetivar a compra da vacina quando a Anvisa autorizar a importação para fins de vacinação em massa.
“A Anvisa autorizou o uso da vacina, mas ainda em fase de testes. E nós precisamos ter segurança de aplicar a vacina em nossa gente. Por isso, necessitamos da aprovação definitiva da Anvisa para comprar e vacinar em massa a nossa população. Esse também é o entendimento dos demais governadores que também querem mais doses de vacina para seus estados”, ressaltou o governador Mauro Carlesse que mesmo estando no Jalapão, fez questão de participar da reunião devido ao interesse em adquirir as vacinas para a população tocantinense.
O secretário de Estado da Saúde, Edgar Tollini, também participou da reunião.
Entenda a decisão da Anvisa
Na noite dessa sexta-feira, 4, a Diretoria Colegiada da Anvisa, após pouco mais de 7 horas de reunião, por 4 votos a 1, autorizou a importação da vacina Sputnik V em quantidades específicas e para fins de distribuição e uso em condições controladas determinadas pela Agência. Na prática, uma parte do quantitativo de doses da vacina poderá ser importada no primeiro momento para ser utilizada dentro de um estudo de efetividade a ser seguido pelos estados requerentes. Ou seja, ainda não é uma autorização para vacinação em massa, mas para testes.
Conforme a autorização da Anvisa, as principais condições para o uso da Sputnik preveem pontos como: importação somente de vacinas das fábricas inspecionadas pela Anvisa na Rússia (Generium e Pharmstandard UfaVita); obrigação de análise lote a lote que comprove ausência de vírus replicantes e outras características de qualidade; e notificação de eventos adversos graves em até 24 horas. As notificações de eventos adversos serão analisadas pelas áreas de Fiscalização e monitoramento da Agência.
Votaram a favor do relator Alex Campos, o diretor-presidente da Anvisa, Antonio Barra Torres; o diretor Romison Rodrigues Mota e a diretora Meiruze Sousa Freitas. A diretora Cristiane Jourdan Gomes votou contra.
O relator destacou que a importação foi autorizada por força da Lei 14.124/2021 e que por isso os aspectos de qualidade, segurança e eficácia da vacina Sputnik V foram atestados por meio do registro concedido pela autoridade sanitária da Rússia. Ou seja, não foram considerados os aspectos regulatórios ordinários que são aplicados pelas áreas técnicas da Anvisa para assegurar a comprovação de qualidade, segurança e eficácia de vacinas tanto na concessão de registro como na autorização de uso emergencial no Brasil.
Com a decisão, fica autorizada a importação excepcional e temporária correspondente a doses para vacinação de 1% da população de cada um dos estados requerentes. Somente após essa fase é que a Anvisa vai analisar os dados de monitoramento do uso da vacina para poder avaliar os próximos quantitativos a serem importados.
Dessa forma, a importação e o uso das vacinas poderão ser suspensos caso o pedido de uso emergencial em análise pela Anvisa ou pela Organização Mundial da Saúde (OMS) seja negado. Ou ainda, pode ser suspenso com base em informações provenientes do controle e do monitoramento do uso da vacina Sputnik V no Brasil.