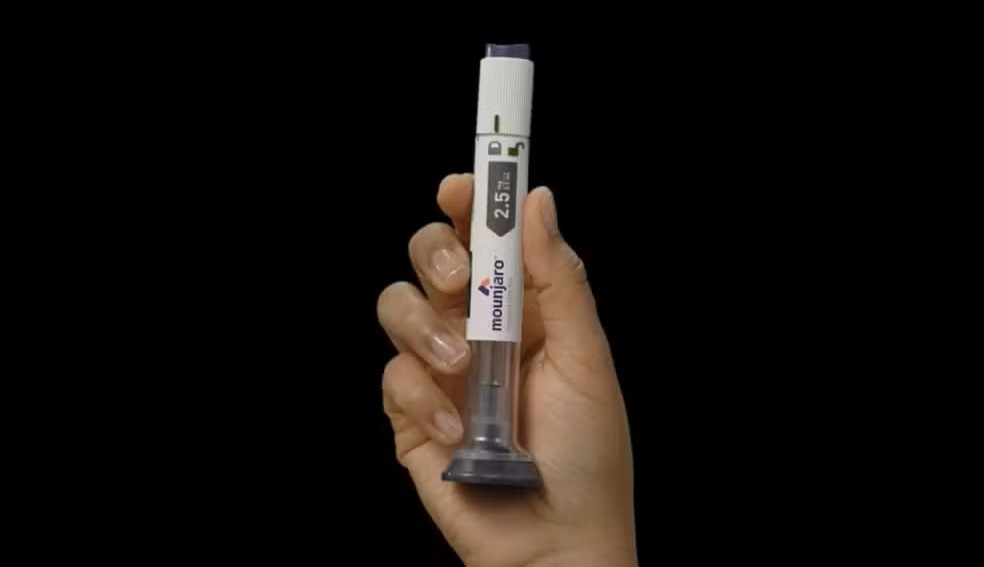
A Agência Nacional de Vigilância Sanitária aprovou o registro de uma nova versão do Mounjaro, medicamento utilizado no tratamento do diabetes tipo 2. A decisão foi publicada no Diário Oficial da União desta quarta-feira (18).
Batizada de Mounjaro Multidose, a nova apresentação permite o uso de uma mesma caneta aplicadora em mais de uma dose, ao contrário do modelo tradicional, que é descartável após uma única aplicação.
A autorização está prevista na Resolução-RE nº 1.041, emitida pela Gerência-Geral de Medicamentos, e foi concedida à farmacêutica Eli Lilly do Brasil. O medicamento tem como princípio ativo a tirzepatida.
O registro inclui seis concentrações diferentes, todas em solução injetável de uso subcutâneo: 4,17 mg/mL, 8,33 mg/mL, 12,5 mg/mL, 16,7 mg/mL, 20,8 mg/mL e 25 mg/mL. A validade do registro é de 24 meses.
Na prática, a principal mudança é o formato multidose, que permite múltiplas aplicações com a mesma caneta, o que pode facilitar o uso pelos pacientes.
A tirzepatida atua em hormônios ligados ao controle da glicose e do apetite, contribuindo tanto para o tratamento do diabetes quanto para a redução de peso.
Com a aprovação, a nova versão já está autorizada para comercialização no Brasil. No entanto, a disponibilização nas farmácias ainda depende de etapas como definição de preço e estratégia de lançamento pela empresa.